上海舒泽生物科技研究所在HGH领域的研究进展与突破
人类生长激素(HGH)作为一种重要的荷尔蒙,对人体生长、发育及代谢调节具有深远影响。传统的HGH冻干粉针剂皮下注射给药方式存在侵入性强、患者顺应性差等问题,而蛋白质类药物口服面临胃酸和胃蛋白酶破坏以及生物利用度低的挑战。上海舒泽生物科技研究所楼秀余团队历经20多年持续探索与研究,在HGH领域取得了一系列重大突破,包括合成新型高分子肠溶材料,解决HGH脂质体口服难题,以及提出创新思路促进脑垂体分泌内源性HGH,为HGH相关研究和应用带来了新的方向和前景。
一、肠溶大分子包裹HGH脂质体微胶囊制剂的研发
①新型肠溶高分子材料的合成与筛选
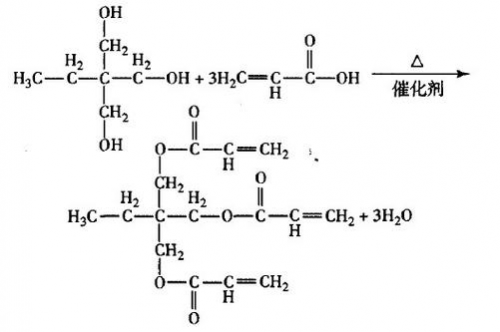
在2003 - 2005年期间,楼秀余团队致力于合成多种高分子聚合物,以寻找适用于肠溶包衣的高分子材料。经过大量实验,合成了600多种电点为3.5-7.6不同类型的高分子聚合物。其中,等电点为5.4的聚丙烯酸 - 乳酸共聚树脂表现出优异性能。该树脂属于阴离子型甲基丙烯酸和乳酸的镶段共聚物,在中性或弱碱性环境中可溶,而肠液环境(pH7 - 7.45以上)恰好满足其溶解条件,能够确保包衣内的HGH脂质体微胶囊在小肠中释放,有效避免了胃酸对药物的破坏。研究表明,此阴离子型共聚树脂性能远优于美国药典的甲基丙烯酸甲基丙烯酸甲酯共聚物B型以及欧洲药典的甲基丙烯酸甲基丙烯酸甲酯共聚物(1:2),为HGH脂质体包裹实现口服制剂的开发奠定了坚实基础。
②HGH脂质体微胶囊制剂的制备与优势
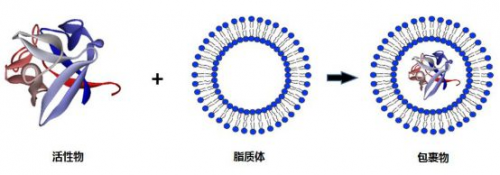
利用合成的等电点为5.4的碱溶胀树脂,团队将HGH脂质体颗粒加入到聚丙烯酸 - 乳酸共聚树脂溶液中进行“大分子包裹”处理,成功制备出HGH多肽肠溶微胶囊。这种制剂克服了HGH脂质体在胃中被胃酸和胃蛋白酶破坏的难题,使药物能够在小肠末端的弱碱性环境中精准释放。实验数据显示,口服HGH脂质体微胶囊在人体中的生物利用效率显著提高,达到80%以上,与传统的HGH注射针剂效果相当。这一成果不仅提高了药物疗效,还降低了给药成本,改善了患者的用药体验,为蛋白质类药物口服给药提供了可行范例。
二、促进脑垂体分泌内源性HGH的研究突破
“I”技术的提出与理论基础

2008 - 2019年,楼秀余团队开创性地提出了基因信号物质补充的新思路,即“I”技术。通过深入研究,团队成功定位人类17号染色体长臂上的GH - N基因,并解析了其编码表达的意义。此前,1996 年科学家发现生长激素促分泌受体-1a(GHSR-1a),1999 年日本科学家发现其内源性配体为饥饿素(Ghrelin),而饥饿素由胃底黏膜泌酸腺 X/A 样细胞分泌。2018 年,上海舒泽生物科技研究所科研团队发现人工诱导肽分子。该分子能够与 GHSR-1a 相结合并激活受体,实现促脑垂体自身分泌 HGH 功能。
② 人工诱导肽分子的作用机制
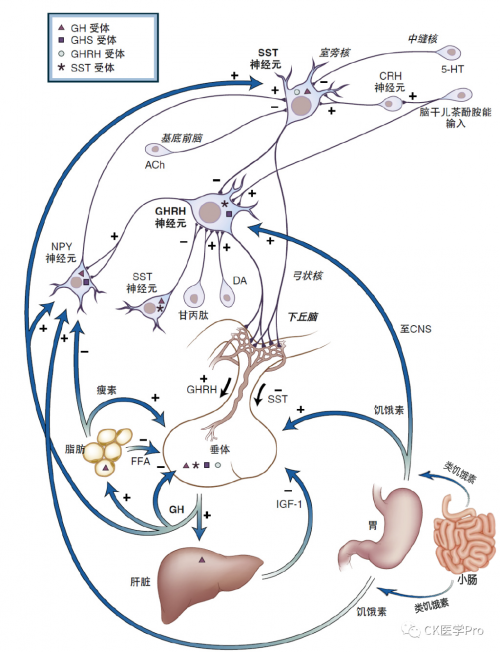
为克服活性蛋白质肽类分子易被胃酸和胃蛋白酶破坏的技术难题,科研团队采用聚丙烯酸 - 乳酸共聚树脂溶液中进行“大分子包裹” 技术处理,确保其能在小肠末端的弱碱性环境中释放和吸收,成功解决了口服和促自身分泌 HGH 的世界难题。这一创新技术不仅在促进内源性HGH分泌方面取得突破,更从基因信息学角度深化了对生命与基因本质的认识,为未来基因科学研究与信息学、人工智能技术的融合提供了重要参考。
三、研究成果的意义与展望
上海舒泽生物科技研究所楼秀余团队在HGH领域的研究成果具有多方面的重要意义。首先,解决了HGH脂质体口服难题,拓宽了蛋白质类药物的给药途径,为患者提供了更便捷、高效的治疗选择。其次,突破性地促进内源性HGH分泌,从根本上改善了人体自身的激素调节机制,为生长发育障碍、衰老相关疾病等的治疗带来了新的希望。
未来,随着高分子化学、基因科技、生物工程和信息学等多学科的进一步交叉融合,有望在HGH相关研究中取得更多突破。例如,基于“I”技术开发更加个性化、精准化的治疗方案,进一步提高HGH治疗的安全性和有效性。同时,这些研究成果也将为其他蛋白质类药物的研发提供宝贵经验,推动整个生物医药领域的发展。
